当前最新:2022中国新冠药物产业链现状与发展前景分析
新冠药物市场前景如何?7月25日,国家药监局根据《药品管理法》相关规定,按照药品特别审批程序,进行应急审评审批,附条件批准河南真实生物科技有限公司阿兹夫定片增加治疗新冠病毒肺炎适应症注册申请。
2022中国新冠药物产业链现状与发展前景分析
我国首个自主知识产权口服抗新冠药物阿兹夫定,从研发、原料药生产、制剂生产到销售总部等全产业链已经具备落地河南的基本条件,此举标志着河南省实施创新驱动、科教兴省、人才强省战略取得标志性突破。
 (相关资料图)
(相关资料图)
一条新药产业链的完整形成,要经过产品研发、临床试验、生产资质审批、原料药及辅料关联审批、产品上市审批、经营销售资质审批等多个环节。而这一切,均建立在严格的法律许可、科学的技术验证、严谨的体系规范和成熟的生产工艺基础之上。
根据中研产业研究院《2022-2027年中国新冠药物行业市场全面分析及发展趋势调研报告》显示:
资料显示,阿兹夫定片是我国自主研发的口服小分子新冠病毒肺炎治疗药物。2021年7月20日,国家药监局已附条件批准本品与其他逆转录酶抑制剂联用治疗高病毒载量的成年HIV-1感染患者。
据了解,阿兹夫定片大规模上市所需的企业生产经营资质、产品注册信息变更和数据转移、原料药生产等关键问题全部得到解决。截至目前,阿兹夫定片相关注册信息数据已顺利转移到我省,企业立足河南发展壮大的基础更加牢固。新乡制药股份有限公司新建原料药生产线取得生产许可,原料生产得到充分保障。河南真实生物科技有限公司取得附条件生产许可,已具备制剂生产资质。同时,省药监局向真实生物发放了药品经营许可证,为企业建设产品销售网络提供了条件。
河南省生物医药产业基础较好,在生物育种、现代中药、新型疫苗、医用耗材等领域具有较强竞争力,但在创新药领域发展、突破的势头一直不够强劲。全省有300多家药品生产企业,每年获批的药品文号在20个左右,其中以仿制药居多。国家药监局发布的《2021年度药品审评报告》显示,2021年全国共受理新药临床试验申请2412件、新药上市许可申请389件,审评通过47个创新药,其中,获得批准的全新化合物结构创新的1类新药寥寥无几,创新药上市获批的难度和价值可想而知。
2022年7月25日,国家药监局根据《药品管理法》相关规定,按照药品特别审批程序,进行应急审评审批,附条件批准河南真实生物科技有限公司阿兹夫定片增加治疗新冠病毒肺炎适应症注册申请。此次为附条件批准新增适应症,用于治疗普通型新型冠状病毒肺炎(COVID-19)成年患者。患者应在医师指导下严格按说明书用药。国家药监局要求上市许可持有人继续开展相关研究工作,限期完成附条件的要求,及时提交后续研究结果。
此前,真实生物先后与新华制药、华润双鹤等签订委托生产协议。复星医药7月25日晚间发布公告,控股子公司复星医药产业与真实生物签订《战略合作协议》,双方就推进联合开发并由复星医药产业独家商业化阿兹夫定等事宜达成战略合作,本次合作领域包括新冠病毒、艾滋病治疗及预防领域。
想了解更多新型储能行业研究具体分析,可点击中研产业研究院《2022-2027年中国新冠疫苗行业市场全面分析及发展趋势调研报告》.报告对行业相关各种因素进行具体调查、研究、分析,洞察行业今后的发展方向、行业竞争格局的演变趋势以及技术标准、市场规模、潜在问题与行业发展的症结所在,评估行业投资价值、效果效益程度,提出建设性意见建议,为行业投资决策者和企业经营者提供参考依据。
-
 当前最新:2022中国新冠药物产业链现状与发展前景分析 新冠药物市场前景如何?7月25日,国家药监局根据《药品管理法》相关规定,按照药品特别审批程序,进行应急审评审批,附条件批准河南真实生物科
当前最新:2022中国新冠药物产业链现状与发展前景分析 新冠药物市场前景如何?7月25日,国家药监局根据《药品管理法》相关规定,按照药品特别审批程序,进行应急审评审批,附条件批准河南真实生物科 -
 保持恢复发展势头 商务部落实已出台措施促进消费持续恢复 7日,商务部举行的网上例行新闻发布会上,商务部新闻发言人束珏婷表示,5月以来国内消费保持恢复发展势头。商务部将落实好已出台的稳增长、
保持恢复发展势头 商务部落实已出台措施促进消费持续恢复 7日,商务部举行的网上例行新闻发布会上,商务部新闻发言人束珏婷表示,5月以来国内消费保持恢复发展势头。商务部将落实好已出台的稳增长、 -
 百强房企6月销售数据出炉 6月起始回暖或成主旋律 7月7日,资本邦了解到,近期公布的百强房企6月销售金额环比出现显著改善。根据克而瑞最新数据,6月,TOP100房企实现销售金额7329 7亿元,环
百强房企6月销售数据出炉 6月起始回暖或成主旋律 7月7日,资本邦了解到,近期公布的百强房企6月销售金额环比出现显著改善。根据克而瑞最新数据,6月,TOP100房企实现销售金额7329 7亿元,环 -
 游戏驿站宣布1:4拆股计划 7月22日开始交易 7月7日,资本邦了解到,美股上市公司游戏驿站(GME US)宣布将其股票将按1比4的比例进行拆分,在7月18日交易结束时登记在册的股东每持有1股A
游戏驿站宣布1:4拆股计划 7月22日开始交易 7月7日,资本邦了解到,美股上市公司游戏驿站(GME US)宣布将其股票将按1比4的比例进行拆分,在7月18日交易结束时登记在册的股东每持有1股A -
 北京农商银行推出63项举措 助力企业稳健发展 日前,北京农商银行迅速响应制定金融助企纾困工作措施,快速出台《北京农商银行落实疫情防控和稳定经济增长工作方案》,推出63项举措,全方
北京农商银行推出63项举措 助力企业稳健发展 日前,北京农商银行迅速响应制定金融助企纾困工作措施,快速出台《北京农商银行落实疫情防控和稳定经济增长工作方案》,推出63项举措,全方 -
 【环球时快讯】秦创原铜川创新驱动平台企业完成自主研发国产碳监测仪器设备比对 近日,铜川市碳监测项目组赴陕西关中平原区域生态环境变化与综合治理国家野外科学观测研究站,对监测高精度温室气体拟采用的光声光...
【环球时快讯】秦创原铜川创新驱动平台企业完成自主研发国产碳监测仪器设备比对 近日,铜川市碳监测项目组赴陕西关中平原区域生态环境变化与综合治理国家野外科学观测研究站,对监测高精度温室气体拟采用的光声光...
-
 当前最新:2022中国新冠药物产业链现状与发展前景分析 新冠药物市场前景如何?7月25日,国家药监局根据《药品管理法》相关规定,按照药品特别审批程序,进行应急审评审批,附条件批准河南真实生物科
当前最新:2022中国新冠药物产业链现状与发展前景分析 新冠药物市场前景如何?7月25日,国家药监局根据《药品管理法》相关规定,按照药品特别审批程序,进行应急审评审批,附条件批准河南真实生物科 -
 世界要闻:社保基金二季度重仓股名单(附股) 财报季,社保基金持股动向曝光!二季度末社保基金共现身5只个股前十大流通股东榜,新进2只,增持2只。证券时报& 183;数据宝统计显示,...
世界要闻:社保基金二季度重仓股名单(附股) 财报季,社保基金持股动向曝光!二季度末社保基金共现身5只个股前十大流通股东榜,新进2只,增持2只。证券时报& 183;数据宝统计显示,... -
 天天最资讯丨阿里巴巴宣布转换至双重上市 或有望纳入港股通 阿里巴巴集团控股有限公司今日早间发布公告称,董事会已授权公司管理层申请在香港联交所主板改变上市地位为主要上市。注:公告根据以上...
天天最资讯丨阿里巴巴宣布转换至双重上市 或有望纳入港股通 阿里巴巴集团控股有限公司今日早间发布公告称,董事会已授权公司管理层申请在香港联交所主板改变上市地位为主要上市。注:公告根据以上... -
 天天最新:流向依旧反复不定 “聪明钱”正抄底?最新增减持板块一览 7月25日,两市股指盘中弱势震荡下探,截至收盘,沪指跌0 6%,深成指跌0 83%,创业板指跌1 18%。房地产板块全天强势,猴痘概念、厨卫电器、贵金
天天最新:流向依旧反复不定 “聪明钱”正抄底?最新增减持板块一览 7月25日,两市股指盘中弱势震荡下探,截至收盘,沪指跌0 6%,深成指跌0 83%,创业板指跌1 18%。房地产板块全天强势,猴痘概念、厨卫电器、贵金 -
 环球通讯!大罚单频现!年内17家信托公司被罚超4200万 中铁信托、雪松信托等居罚单前列 近日,多家信托公司被罚,年内收罚单的信托公司再添新案例。财联社不完全统计发现,以公告日期来看,截至发稿,年内共计有17家信托公司...
环球通讯!大罚单频现!年内17家信托公司被罚超4200万 中铁信托、雪松信托等居罚单前列 近日,多家信托公司被罚,年内收罚单的信托公司再添新案例。财联社不完全统计发现,以公告日期来看,截至发稿,年内共计有17家信托公司... -
 每日焦点!建议持续追踪新老基建相关BIPV、高速光伏等品种 一、市场回顾昨日市场主要是在新能源赛道品种拖累下、脉冲向下,而低位的医药、地产、家电走出防御表现。新能源大跌一方面是获利盘释放...
每日焦点!建议持续追踪新老基建相关BIPV、高速光伏等品种 一、市场回顾昨日市场主要是在新能源赛道品种拖累下、脉冲向下,而低位的医药、地产、家电走出防御表现。新能源大跌一方面是获利盘释放... -
 保持恢复发展势头 商务部落实已出台措施促进消费持续恢复 7日,商务部举行的网上例行新闻发布会上,商务部新闻发言人束珏婷表示,5月以来国内消费保持恢复发展势头。商务部将落实好已出台的稳增长、
保持恢复发展势头 商务部落实已出台措施促进消费持续恢复 7日,商务部举行的网上例行新闻发布会上,商务部新闻发言人束珏婷表示,5月以来国内消费保持恢复发展势头。商务部将落实好已出台的稳增长、 -
 广东对首批27.9万家符合条件的“免申即享”企业发放6.1亿补贴 为进一步支持制造业中小企业和个体工商户纾困发展,广东地区(不含深圳)近日对首批27 9万家符合条件的免申即享企业发放6 1亿补贴。补贴标准
广东对首批27.9万家符合条件的“免申即享”企业发放6.1亿补贴 为进一步支持制造业中小企业和个体工商户纾困发展,广东地区(不含深圳)近日对首批27 9万家符合条件的免申即享企业发放6 1亿补贴。补贴标准 -
 政策惠及面达100%!天津12.47万户小微企业享受税收优惠 天津市税务局最新发布的2021年度企业所得税汇算清缴数据显示:本市有12 47万户小微企业在年度汇算清缴中享受优惠65 23亿元,政策惠及面达10
政策惠及面达100%!天津12.47万户小微企业享受税收优惠 天津市税务局最新发布的2021年度企业所得税汇算清缴数据显示:本市有12 47万户小微企业在年度汇算清缴中享受优惠65 23亿元,政策惠及面达10 -
 天津调整退休人员基本养老金 调整后全市237万人将受益 日前,市人社局、市财政局下发通知,从2022年1月1日起,同步调整企业与机关事业单位2021年12月31日前退休、退职人员的基本养老金。具体办法
天津调整退休人员基本养老金 调整后全市237万人将受益 日前,市人社局、市财政局下发通知,从2022年1月1日起,同步调整企业与机关事业单位2021年12月31日前退休、退职人员的基本养老金。具体办法 -
 网购售后要求开箱视频引争议 直播间购物应注意退货的适用范围 如今,网购已经成为人们日常生活中的一个重要组成部分。近日,广州有市民网购后需要退款,却被商家要求提供开箱视频引发热议。商家要求消费
网购售后要求开箱视频引争议 直播间购物应注意退货的适用范围 如今,网购已经成为人们日常生活中的一个重要组成部分。近日,广州有市民网购后需要退款,却被商家要求提供开箱视频引发热议。商家要求消费 -
 华瑞银行股权再遇变动 股权频遭“法拍”民营银行发生了什么 二股东股权转让尚未完成,上海华瑞银行又有超两亿股股权将于下月被拍卖。据了解,民营银行股权进行司法拍卖并非个例,近年来时有发生。这些
华瑞银行股权再遇变动 股权频遭“法拍”民营银行发生了什么 二股东股权转让尚未完成,上海华瑞银行又有超两亿股股权将于下月被拍卖。据了解,民营银行股权进行司法拍卖并非个例,近年来时有发生。这些 -
 外源性资本补充受限 民营银行该如何“补血” 在试点启动的第八个年头,民营银行开启了第二轮融资。近日,浙江银保监局发布消息称,同意浙江网商银行增资扩股方案。这是网商银行2015年成
外源性资本补充受限 民营银行该如何“补血” 在试点启动的第八个年头,民营银行开启了第二轮融资。近日,浙江银保监局发布消息称,同意浙江网商银行增资扩股方案。这是网商银行2015年成 -
 拟募资6.65亿元!海泰新能北交所IPO获注册批复 7月7日,资本邦了解到,海泰新能(835985 NQ)近日收到关于同意唐山海泰新能科技股份有限公司向不特定合格投资者公开发行股票注册的批复。海
拟募资6.65亿元!海泰新能北交所IPO获注册批复 7月7日,资本邦了解到,海泰新能(835985 NQ)近日收到关于同意唐山海泰新能科技股份有限公司向不特定合格投资者公开发行股票注册的批复。海 -
 百强房企6月销售数据出炉 6月起始回暖或成主旋律 7月7日,资本邦了解到,近期公布的百强房企6月销售金额环比出现显著改善。根据克而瑞最新数据,6月,TOP100房企实现销售金额7329 7亿元,环
百强房企6月销售数据出炉 6月起始回暖或成主旋律 7月7日,资本邦了解到,近期公布的百强房企6月销售金额环比出现显著改善。根据克而瑞最新数据,6月,TOP100房企实现销售金额7329 7亿元,环 -
 铭赛科技撤回科创板上市申请 预计2021年业绩不及预期 近日,资本邦了解到,常州铭赛机器人科技股份有限公司(下称铭赛科技)又披露首次公开发行股票并上市辅导的备案报告,本次辅导协议签署时间为
铭赛科技撤回科创板上市申请 预计2021年业绩不及预期 近日,资本邦了解到,常州铭赛机器人科技股份有限公司(下称铭赛科技)又披露首次公开发行股票并上市辅导的备案报告,本次辅导协议签署时间为 -
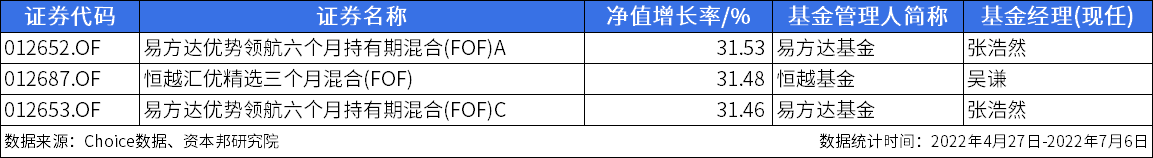 多只FOF基金业绩反弹超30% 首位业绩分化已超45% 7月7日,资本邦了解到,市场自今年4月27日低点以来,持续反弹。基金方面,新能源主题基金呈现大幅回血,由此,部分重仓新能源基金的FOF产品
多只FOF基金业绩反弹超30% 首位业绩分化已超45% 7月7日,资本邦了解到,市场自今年4月27日低点以来,持续反弹。基金方面,新能源主题基金呈现大幅回血,由此,部分重仓新能源基金的FOF产品 -
 天天讯息:*ST亚联录得13天12板 *ST亚联再度涨停,13个交易日内录得12个涨停,累计涨幅为73 45%,累计换手率为95 53%。截至09:34,该股今日成交量909 62万股,成交金额3491 08
天天讯息:*ST亚联录得13天12板 *ST亚联再度涨停,13个交易日内录得12个涨停,累计涨幅为73 45%,累计换手率为95 53%。截至09:34,该股今日成交量909 62万股,成交金额3491 08 -
 环球速讯:太阳电缆录得5天3板 太阳电缆再度涨停,5个交易日内录得3个涨停,累计涨幅为33 58%,累计换手率为51 53%。截至09:36,该股今日成交量3134 51万股,成交金额3 23亿
环球速讯:太阳电缆录得5天3板 太阳电缆再度涨停,5个交易日内录得3个涨停,累计涨幅为33 58%,累计换手率为51 53%。截至09:36,该股今日成交量3134 51万股,成交金额3 23亿 -
 天天视点!天汽模最新筹码趋于集中 天汽模7月25日在交易所互动平台中披露,截至7月20日公司股东户数为72528户,较上期(7月10日)减少4206户,环比降幅为5 48%。证券时报& 183;数据
天天视点!天汽模最新筹码趋于集中 天汽模7月25日在交易所互动平台中披露,截至7月20日公司股东户数为72528户,较上期(7月10日)减少4206户,环比降幅为5 48%。证券时报& 183;数据 -
 世界今热点:中国气象局部署保秋粮丰收气象服务工作 据中国气象局7月26日消息,中国气象局近日印发《全力以赴保秋粮丰收气象服务工作方案》(以下简称《方案》),要求坚持需求牵引,做好分类...
世界今热点:中国气象局部署保秋粮丰收气象服务工作 据中国气象局7月26日消息,中国气象局近日印发《全力以赴保秋粮丰收气象服务工作方案》(以下简称《方案》),要求坚持需求牵引,做好分类... -
 资讯:美的集团、TCL中环等19股获北向资金增持额超亿元 据wind统计显示,7月25日共有542只个股获北向资金持股量环比上一个交易日增加。以增持的股份数量和当日收盘价为基准进行测算,加仓股中,增持
资讯:美的集团、TCL中环等19股获北向资金增持额超亿元 据wind统计显示,7月25日共有542只个股获北向资金持股量环比上一个交易日增加。以增持的股份数量和当日收盘价为基准进行测算,加仓股中,增持 -
 陕西煤业发布半年报业绩预告 预计业绩大幅上升 7月7日,资本邦了解到,A股上市公司陕西煤业(代码:601225 SH)发布半年报业绩预告,公司预计2022年1-6月业绩大幅上升,归属于上市公司股东
陕西煤业发布半年报业绩预告 预计业绩大幅上升 7月7日,资本邦了解到,A股上市公司陕西煤业(代码:601225 SH)发布半年报业绩预告,公司预计2022年1-6月业绩大幅上升,归属于上市公司股东 -
 企业环境信息公众一目了然 深圳推出年度报告编制模板 近日,深圳市生态环境局发布了首份具有深圳特色的企业环境信息披露年报。据了解,为实现信息披露模板标准化,提升信息披露的公信力与披露数
企业环境信息公众一目了然 深圳推出年度报告编制模板 近日,深圳市生态环境局发布了首份具有深圳特色的企业环境信息披露年报。据了解,为实现信息披露模板标准化,提升信息披露的公信力与披露数 -
 投资43亿元 深圳市新华医院项目主体结构封顶 昨日,深圳市新华医院项目主体结构举行封顶仪式,这意味着该院的主体结构施工已完成,全面转入室内装修。深圳市新华医院是深圳市政府全额投
投资43亿元 深圳市新华医院项目主体结构封顶 昨日,深圳市新华医院项目主体结构举行封顶仪式,这意味着该院的主体结构施工已完成,全面转入室内装修。深圳市新华医院是深圳市政府全额投 -
 深圳助企纾困再出大招 企业可享受留工培训补助 记者从深圳市人力资源和社会保障局获悉,我市助企纾困再出大招,对受疫情严重影响企业,按每名参保职工500元的标准发放一次性留工培训补助
深圳助企纾困再出大招 企业可享受留工培训补助 记者从深圳市人力资源和社会保障局获悉,我市助企纾困再出大招,对受疫情严重影响企业,按每名参保职工500元的标准发放一次性留工培训补助 -
 奥比中光成功登陆科创板 深圳南山区上市企业达195家 聚焦3D感知芯片研发的奥比中光科技集团股份有限公司7月7日登陆科创板,该公司研发了中国第一颗3D感知芯片,被称为3D视觉第一股。至此,南山
奥比中光成功登陆科创板 深圳南山区上市企业达195家 聚焦3D感知芯片研发的奥比中光科技集团股份有限公司7月7日登陆科创板,该公司研发了中国第一颗3D感知芯片,被称为3D视觉第一股。至此,南山 -
 视焦点讯!闯祸了?特斯拉炒币或大亏 又收到一张传票 美科技股也被带崩了 【闯祸了?特斯拉炒币或大亏又收到一张传票美科技股也被带崩了】周一,美股三大指数收盘涨跌不一。美股猴痘概念股大幅走高,GeoVaxLabs涨近150
视焦点讯!闯祸了?特斯拉炒币或大亏 又收到一张传票 美科技股也被带崩了 【闯祸了?特斯拉炒币或大亏又收到一张传票美科技股也被带崩了】周一,美股三大指数收盘涨跌不一。美股猴痘概念股大幅走高,GeoVaxLabs涨近150 -
 世界观点:股票型ETF流动性第一 这只ETF只用了一周完成“逆袭”!背后原因是什么? 继上周五创下单日成交超22亿元的历史记录后,昨日华夏中证1000ETF(159845)热度不减,全天共成交14 82亿元,换手率61 98%,无论是成交额还是换
世界观点:股票型ETF流动性第一 这只ETF只用了一周完成“逆袭”!背后原因是什么? 继上周五创下单日成交超22亿元的历史记录后,昨日华夏中证1000ETF(159845)热度不减,全天共成交14 82亿元,换手率61 98%,无论是成交额还是换 -
 天天微速讯:阿里巴巴:寻求于港交所主要上市 预计年底前将于纽交所及港交所双重... 【阿里巴巴集团寻求于港交所主要上市完成后将于纽约交易所及港交所双重主要上市】阿里巴巴在港交所公告,董事会已授权本公司管理层申请...
天天微速讯:阿里巴巴:寻求于港交所主要上市 预计年底前将于纽交所及港交所双重... 【阿里巴巴集团寻求于港交所主要上市完成后将于纽约交易所及港交所双重主要上市】阿里巴巴在港交所公告,董事会已授权本公司管理层申请...
热门资讯
-
 外源性资本补充受限 民营银行该如何“补血” 在试点启动的第八个年头,民营银行...
外源性资本补充受限 民营银行该如何“补血” 在试点启动的第八个年头,民营银行... -
 天天讯息:*ST亚联录得13天12板 *ST亚联再度涨停,13个交易日内录...
天天讯息:*ST亚联录得13天12板 *ST亚联再度涨停,13个交易日内录... -
 环球速讯:太阳电缆录得5天3板 太阳电缆再度涨停,5个交易日内录...
环球速讯:太阳电缆录得5天3板 太阳电缆再度涨停,5个交易日内录... -
 世界今热点:中国气象局部署保秋粮丰收气象服务工作 据中国气象局7月26日消息,中国气...
世界今热点:中国气象局部署保秋粮丰收气象服务工作 据中国气象局7月26日消息,中国气...
文章排行
图赏
-
 辽宁省农作物播种进度达87.3% 旱田作物播种接近尾声 春争日、夏争时,农时不等人。据最...
辽宁省农作物播种进度达87.3% 旱田作物播种接近尾声 春争日、夏争时,农时不等人。据最... -
 纪录电影《人间世》讲述两个家庭的真实抗癌故事 纪录电影《人间世》于清明节4月3日...
纪录电影《人间世》讲述两个家庭的真实抗癌故事 纪录电影《人间世》于清明节4月3日... -
 国家植物园:“中国鸽子树”珙桐满树繁花犹如白鸽翩翩欲飞 国家植物园(北园)的宿根花卉园里,...
国家植物园:“中国鸽子树”珙桐满树繁花犹如白鸽翩翩欲飞 国家植物园(北园)的宿根花卉园里,... -
 露营+踏青赏花!“五一”假期热门深度游目的地出炉 我已经预订了密云水库附近的民宿,...
露营+踏青赏花!“五一”假期热门深度游目的地出炉 我已经预订了密云水库附近的民宿,...