十三年科研攻关 暨南大学丁克教授团队自主研发新药上市
12月18日,南都记者从暨南大学教授丁克团队获悉,该团队研发的新药奥雷巴替尼(耐立克)正式宣布上市,该药物用于治疗慢性粒性白血病(CML)耐药性,这将极大缓解中国CML耐药患者的无药可用的困境,也有望为全球CML患者带来全新选择。据悉,奥雷巴替尼是中国人自主设计的化合物实体、中国科研机构独立完成成药性评价、中国企业独立完成临床研发的“中国智造药”。
据团队负责人介绍,慢性粒性白血病(CML)是骨髓造血干细胞克隆性增殖形成的恶性肿瘤,占成人白血病的15%,全球年发病率为1.6/10万~2/10万。大多数CML病人可以通过长期服用格列卫,从而实现带瘤生存。然而,相当一部分患者服药几年后,会产生耐药性。
丁克现为暨南大学药学院院长、教授。2006年,他就关注到中国肿瘤患者药物可及性差、治疗成本高昂等问题,决定紧跟临床需求,研发中国人自己的原创新药。2008年,他与中山大学潘景轩教授开展合作,启动对格列卫耐药的新一代抗肿瘤药物研究,并于当年获得国家“863计划”立项支持。
丁克通过基于结构的理性药物设计策略,指导博士生王德平博等在3年时间里设计、合成了数百个全新分子。他仔细评估每个分子的体内外药效、毒性、药代动力学等数据,综合分析构效关系及成药性,反复进行多轮分子结构改造,初步确定奥雷巴替尼(原编号GZD824)是安全、有效的药物候选分子。这距离项目立项已经过去了3年时间。
2012年,经过系统的安全性评估,丁克教授带领团队完成了GZD824的临床前成药性研究的关键数据,充分证明了其有效和安全性。之后,广州顺健生物医药科技有限公司与团队签订了知识产权转让协议,获得了其全球开发权益;丁克团队又花了经过2年多的时间完成了药物的药学、药理学、毒理学等规范性临床前研究,于2015年4月正式向国家药监局提交了临床试验申请,并顺利通过了现场核查。
2021年11月25日,中国国家药监局(NMPA)附条件批准奥瑞巴替尼上市,用于治疗任何酪氨酸激酶抑制剂耐药。据介绍,奥瑞巴替尼是中国第一个,也是唯一一个获批上市的第三代BCR-ABL抑制剂。
“解决临床需求是我们的出发点,也将永远是我们新药研究的着力点。在这条道路上我们将不忘初心、砥砺前行,争取做出更多临床有用的创新药物。”丁克说。
(文章来源:南方都市报)
-
 前三季度完成交通固定资产投资25632亿元 同比增长2% 记者今天从交通运输部获悉,前三季度,交通运输经济运行总体平稳,交通投资、货运量、港口货物吞吐量两年平均增速均在6%左右,其中三季度受
前三季度完成交通固定资产投资25632亿元 同比增长2% 记者今天从交通运输部获悉,前三季度,交通运输经济运行总体平稳,交通投资、货运量、港口货物吞吐量两年平均增速均在6%左右,其中三季度受 -
 1-9月份第一产业投资10395亿元 同比增长14.0% 据国家统计局官网消息,1-9月份,全国固定资产投资(不含农户)397827亿元,同比增长7 3%;比2019年1-9月份增长7 7%,两年平均增长3 8%。其中
1-9月份第一产业投资10395亿元 同比增长14.0% 据国家统计局官网消息,1-9月份,全国固定资产投资(不含农户)397827亿元,同比增长7 3%;比2019年1-9月份增长7 7%,两年平均增长3 8%。其中 -
 1-8月河南省货物贸易保持高速增长 商务运行稳中有进 据河南省商务厅官网消息,2021年1-8月,全省货物贸易保持高速增长,招商引资保持增长态势,消费品市场恢复态势放缓,对外投资大幅增长,商
1-8月河南省货物贸易保持高速增长 商务运行稳中有进 据河南省商务厅官网消息,2021年1-8月,全省货物贸易保持高速增长,招商引资保持增长态势,消费品市场恢复态势放缓,对外投资大幅增长,商 -
 医药板块投资性价比显现 基金公司密集调研医药上市公司 12月14日,资本邦了解到,随着年内的持续调整,此前一直处于高估值的医药板块投资性价比显现,因此基金公司对相关主题基金的布局速度加快。
医药板块投资性价比显现 基金公司密集调研医药上市公司 12月14日,资本邦了解到,随着年内的持续调整,此前一直处于高估值的医药板块投资性价比显现,因此基金公司对相关主题基金的布局速度加快。 -
 稳增长预期确认 中信证券:跨年蓝筹行情预计将延续数月 12月13日,资本邦了解到,上周(12月6日—12月10日),A股在央行宣布全面降准0 5个百分点后,迎来震荡上行,上证指数周涨幅1 63%,深证成指全
稳增长预期确认 中信证券:跨年蓝筹行情预计将延续数月 12月13日,资本邦了解到,上周(12月6日—12月10日),A股在央行宣布全面降准0 5个百分点后,迎来震荡上行,上证指数周涨幅1 63%,深证成指全 -
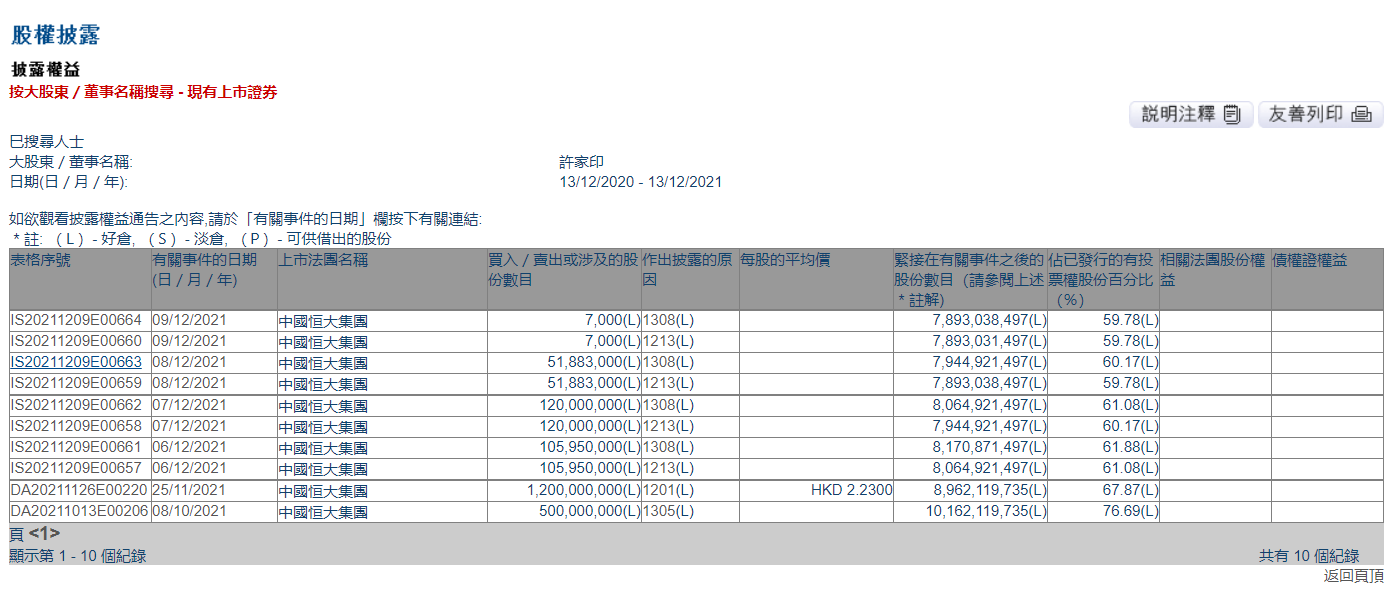 许家印在中国恒大持股比例从61.88%下降至59.78% 12月13日,资本邦了解到,港交所文件显示,依据强制处置事项,12月6日、12月7日、12月8日、12月9日,许家印持续被强制卖出中国恒大1 06亿股
许家印在中国恒大持股比例从61.88%下降至59.78% 12月13日,资本邦了解到,港交所文件显示,依据强制处置事项,12月6日、12月7日、12月8日、12月9日,许家印持续被强制卖出中国恒大1 06亿股
-
十三年科研攻关 暨南大学丁克教授团队自主研发新药上市 12月18日,南都记者从暨南大学教授丁克团队获悉,该团队研发的新药奥雷巴替尼(耐立克)正式宣布上市,该药物用于治疗慢性粒性白血病(CML)耐药性
-
世界最强流深地加速器首批成果发布:中国核天体物理研究达国际先进 中核集团披露,中国首个深地核天体物理实验项目——锦屏深地核天体物理实验首批实验成果发布会18日在北京举行。首批发布4个核天体物理关...
-
武鄂签订9个教育协作项目 名师共享、教研互动、学生互访……12月18日上午,“武鄂同城教育协作”签约仪式在鄂州市学生综合实践基地举办。来自武汉和鄂州的18家单...
-
中金策略:A股关注“稳增长”政策落实 上周五的中央经济工作会议延续了前期政治局会议的精神继续强调“稳增长”。从近期的国内增长数据来看,尽管在地产投资等方面已经出现了...
-
亚辉龙:公司新冠抗原自测检测试剂盒获得欧盟CE认证 【亚辉龙:公司新冠抗原自测检测试剂盒获得欧盟CE认证】亚辉龙(688575)12月19日晚间公告,公司自主研发、生产的新型冠状病毒(SARS-CoV-2)抗原
-
连菊地、接市场 金东风让更多农户“链”上福白菊 烘干、打包、装车……12月15日早,载有5吨福白菊的货车,驶出湖北金兰农业发展有限公司(下简称“金兰公司”),运往广西出口越南。金兰公...
-
2021最受大学生关注雇主榜单发布 Z世代职场人理性务实 12月18日,智联招聘在2021中国年度最佳雇主颁奖典礼上揭晓了“最受大学生关注雇主十强”:腾讯、字节跳动、百度、京东、中国银行、中国...
-
保险业协会就定期寿险、终身寿险、一年期意外伤害保险示范条款公开征求意见 12月17日,中国保险行业协会(以下简称“保险业协会”)发布《定期寿险示范条款(公开征求意见稿)》、《终身寿险示范条款(公开征求意见稿)...
-
“松绑”外资保险经纪公司准入限制 构建新型保险中介市场体系 为进一步明确保险中介市场对外开放有关措施,放宽外资保险中介机构准入条件,12月17日,北京商报记者获悉,银保监会近日印发了《关于明确保险
-
银保监会:外资保险专业中介机构经营业务前应依法依规备案 进一步明确保险中介市场对外开放有关措施,放宽外资保险中介机构准入条件,12月17日,北京商报记者获悉,中国银保监会近日印发了《关于明确保
-
银保监会:大幅取消外资保险经纪公司的准入限制 不再要求股东经营年限、总资产等条件 进一步明确保险中介市场对外开放有关措施,放宽外资保险中介机构准入条件,12月17日,北京商报记者获悉,银保监会近日印发了《关于明确保险中
-
第八届京台公益论坛在京举办 12月16日,第八届京台公益论坛在北京朝林松源酒店以视频连线方式举办,论坛以“疫情防控和社区公益”为主题,邀请来自两岸的4名专家学者...
-
关注职教学生心理健康 北京市职教学会心理健康教育研究会成立 12月17日,北京市职教学会心理健康教育研究会(以下简称“研究会”)成立大会暨心理健康高峰论坛在北京铁路电气化学校举办。北京商报记者...
-
教育部:国内本科以上中外合作办学在读学生超过30万人 12月17日,教育部发布《全国普通高校本科教育教学质量报告(2020年度)》,《报告》指出,疫情期间各高校推进发展了“在地留学教育”,国...
-
“中植系”掌门人、毛阿敏丈夫解直锟猝然离世!万亿金融帝国生变 后续谁来掌舵?... 12月18日晚间,据中植企业集团微信公号消息,中共党员、中植企业集团创始人解直锟先生,因心脏病突发抢救无效,于2021年12月18日9时40分在北京
-
通源石油收关注函:要求说明对控股子公司大德广源进行增资的原因 【通源石油收关注函:要求说明对控股子公司大德广源进行增资的原因】公告显示,截至2021年9月30日,大德广源净资产为-1808 84万元,2021年前三
-
首个全国青少年低碳教育基地在北京学校成立 12月17日,首个全国青少年低碳教育基地在北京学校揭牌成立。在活动现场,中国电子节能技术协会低碳经济专业委员会与北京学校签署了共建低碳校
-
公募小家电持股现分歧 张坤套现长牛苏泊尔 多只基金趁机抄底 一只连涨八年的A股大牛,已淡出明星基金经理张坤的核心持仓。小家电领域厨电行业龙头苏泊尔(002032 SZ)于12月13日披露的最新公告显示,易方达
-
茅台股东嗨了?持股1手以上就可平价购买2瓶飞天 有投资者已接到取酒电话 【17万茅台股东嗨了?持股1手以上就可平价购买2瓶飞天有投资者称已接到取酒电话】贵州茅台股东可以平价购买飞天茅台?18日,有消息称持有贵州
-
2022投什么最赚钱?最全解读:八大明星基金经理发声! 【2022投什么最赚钱?最全解读:八大明星基金经理发声!】距离2021年全年股市行情“收官”只不到两周时间,公募基金即将开启征战2022年...
-
5400万起步!淘宝又有基金公司股权拍卖 【5400万起步!淘宝又有基金公司股权拍卖】连续几年的结构性牛市推动下,绩优公募基金公司股权可谓“香馍馍”,估值随之“水涨船高”,...
-
外资巨头出手!银行、券商这类产品火了 【外资巨头出手!银行、券商这类产品火了】渠道开门红是资管机构每年的“生死战”。如今,外资机构也加入了这一年度大战。所谓的“开门...
-
重庆两江数字经济产业园成立企业上市服务专班 【重庆两江数字经济产业园成立企业上市服务专班】两江数字经济产业园管委会相关负责人现场表示,北交所开市带来重大利好和机遇,园区中...
-
第一届全国博士后创新创业大赛开幕 天津代表团48个项目入围总决赛 12月18日,第一届全国博士后创新创业大赛在广东省佛山市开幕。以“博采科技精华、创新引领未来”为主题,大赛由人力资源和社会保障部、...
-
肇庆海事局联合农业农村局开展2021年渔业船员安全生产技能培训活动 12月14日-17日,肇庆德庆海事处联合德庆县农业农村局对辖区192艘渔船、270余名船员开展渔业船员安全生产技能培训,并免费发放包含救生圈、便携
-
一周要闻回顾|港版SPAC上市规则出炉!明年1月1日起生效;蔚来发布第五款车型 蔚来发布第五款车型:32 8万元起售;贝壳回应浑水做空报告:包含许多事实错误;英国央行加息“抢跑”欧洲央行:不跟;港版SPAC上市规则...
-
“2021年昌平区科技成果转化”系列行动收官 为更好落实《北京市促进科技成果转化条例》,贯彻执行首都“两区”建设重要部署及《昌平区“两区”建设工作方案》,促进昌平区科技创新...
-
大战浑水!贝壳千字文回应做空:存在大量事实错误 12月17日,贝壳在官微发布千字文回应浑水做空报告。贝壳表示,根据对报告的初步审阅和评估,公司认为该报告毫无事实依据,存在大量事实错误、
-
北向资金大调仓!加仓“券茅”逾40亿元 减仓“药茅”超20亿元 Choice数据显示,本周北向资金累计净流入114 67亿元,其中沪股通资金净流入69 53亿元、深股通资金净流入45 14亿元。本周有74只股票新纳入沪、
-
这些脑洞大开的“冷”职业 你想尝试吗? 【这些脑洞大开的“冷”职业你想尝试吗?】近日,工人日报融媒体中心联合中国劳动关系学院劳动教育学院、淘宝在工人日报微博等新媒体平...
热门资讯
-
 前三季度完成交通固定资产投资25632亿元 同比增长2% 记者今天从交通运输部获悉,前三季...
前三季度完成交通固定资产投资25632亿元 同比增长2% 记者今天从交通运输部获悉,前三季... -
 1-9月份第一产业投资10395亿元 同比增长14.0% 据国家统计局官网消息,1-9月份,...
1-9月份第一产业投资10395亿元 同比增长14.0% 据国家统计局官网消息,1-9月份,... -
 1-8月河南省货物贸易保持高速增长 商务运行稳中有进 据河南省商务厅官网消息,2021年1-...
1-8月河南省货物贸易保持高速增长 商务运行稳中有进 据河南省商务厅官网消息,2021年1-... -
 医药板块投资性价比显现 基金公司密集调研医药上市公司 12月14日,资本邦了解到,随着年内...
医药板块投资性价比显现 基金公司密集调研医药上市公司 12月14日,资本邦了解到,随着年内...
文章排行
图赏
-
 拓荆科技针对科创板第二轮问询相关问题进行问询回复 盈利能力不足、产品类型单一且周转...
拓荆科技针对科创板第二轮问询相关问题进行问询回复 盈利能力不足、产品类型单一且周转... -
 立讯精密涨6.32%目前报价36.99元 这家企业主要是干什么的? 据最新消息显示,立讯精密涨6 32%...
立讯精密涨6.32%目前报价36.99元 这家企业主要是干什么的? 据最新消息显示,立讯精密涨6 32%... -
 国漫多利好迈入黄金期 头部动漫公司扎堆IPO 今年以来,动漫市场绽放异彩。暑期...
国漫多利好迈入黄金期 头部动漫公司扎堆IPO 今年以来,动漫市场绽放异彩。暑期... -
 4月1日起 北京市燃油车不得占用充电专用泊位 充电站必须配专人巡检 今日,记者从北京市市场监管局网站...
4月1日起 北京市燃油车不得占用充电专用泊位 充电站必须配专人巡检 今日,记者从北京市市场监管局网站...