中国抗体-B(03681.HK):SM17新药研究申请获FDA受理
来源:格隆汇 时间:2022-02-16 19:22:25
中国抗体-B(03681.HK)宣布,于2022年2月11日(美国东部当地时间),公司已就治疗哮喘的第一类(First-in-Class)治疗产品SM17(注射用人源化抗IL17RB单克隆抗体),提交新药研究申请(“IND”),有关申请已获美国食品药品监督管理局(U.S.Foodand Drug Administration,“FDA”)受理。一旦新药研究申请获FDA批准,公司计划最早于2022年第一季度在美国启动首次人体临床(FIH)研究。
SM17为以IL-17RB为靶点的人源化IgG4-κ单克隆抗体,IL-17RB则是属于IL-17受体家族的一种I型单跨膜糖蛋白。SM17结合IL-17RB后,可抑制由一类被称为“警戒素”的细胞因子导致的Th2细胞相关免疫反应,而“警戒素”已被证明与过敏性疾病的病理过程及气道细胞的病毒感染反应有关。患有未受控制的严重哮喘的患者,会承受哮喘反复发作及住院的风险;而未受控制的严重哮喘疾病会引发群体死亡率╱患病率升高、生活质素下降以及医疗支出增加。目前已获批上市的严重哮喘疗法(包括生物制剂),可一定程度降低哮喘年度发作率。然而,严重哮喘的有效治疗仍存在未满足的医疗需求,尤其是对当前疗法无应答的患者而言。作为哮喘治疗的新路径,靶向Th2炎性细胞因子通路上游介质(例如“警戒素”)的疗法,预计将对气道炎症相关的病理变化产生更广谱的作用,从而较现有疗法更为有效地控制哮喘症状;目前已有针对警戒素相关信号通路,与SM17具有相若作用机制的严重哮喘疗法获FDA批准。
(文章来源:格隆汇)
关键词: 中国抗体-B
-
 顶流不牛了 景顺长城刘彦春正式掉出“千亿”梯队 今年市场走弱,令不少明星基金经理神话破灭,中欧基金的葛兰、景顺长城的刘彦春等纷纷跌落神坛。根据同花顺数据统计,截至上周末,最近一年
顶流不牛了 景顺长城刘彦春正式掉出“千亿”梯队 今年市场走弱,令不少明星基金经理神话破灭,中欧基金的葛兰、景顺长城的刘彦春等纷纷跌落神坛。根据同花顺数据统计,截至上周末,最近一年 -
 蓝筹股上涨赛道股大跌 A股呈现明显分化走势 虎年首周,A股呈现明显的分化走势。以金融等蓝筹股为代表的上证50单周上涨2 91%,而以成长股为代表的创业板大跌5 59%。一边是部分金融、地
蓝筹股上涨赛道股大跌 A股呈现明显分化走势 虎年首周,A股呈现明显的分化走势。以金融等蓝筹股为代表的上证50单周上涨2 91%,而以成长股为代表的创业板大跌5 59%。一边是部分金融、地 -
 信达生物股价大幅拉升至34.25港元 被要求补充额外临床试验 2月11日,资本邦了解到,港股公司信达生物(01801 HK)早盘低开3 95%报32 8港元 股,截至发稿,股价大幅拉升至34 25港元,微涨0 29%,最新市
信达生物股价大幅拉升至34.25港元 被要求补充额外临床试验 2月11日,资本邦了解到,港股公司信达生物(01801 HK)早盘低开3 95%报32 8港元 股,截至发稿,股价大幅拉升至34 25港元,微涨0 29%,最新市 -
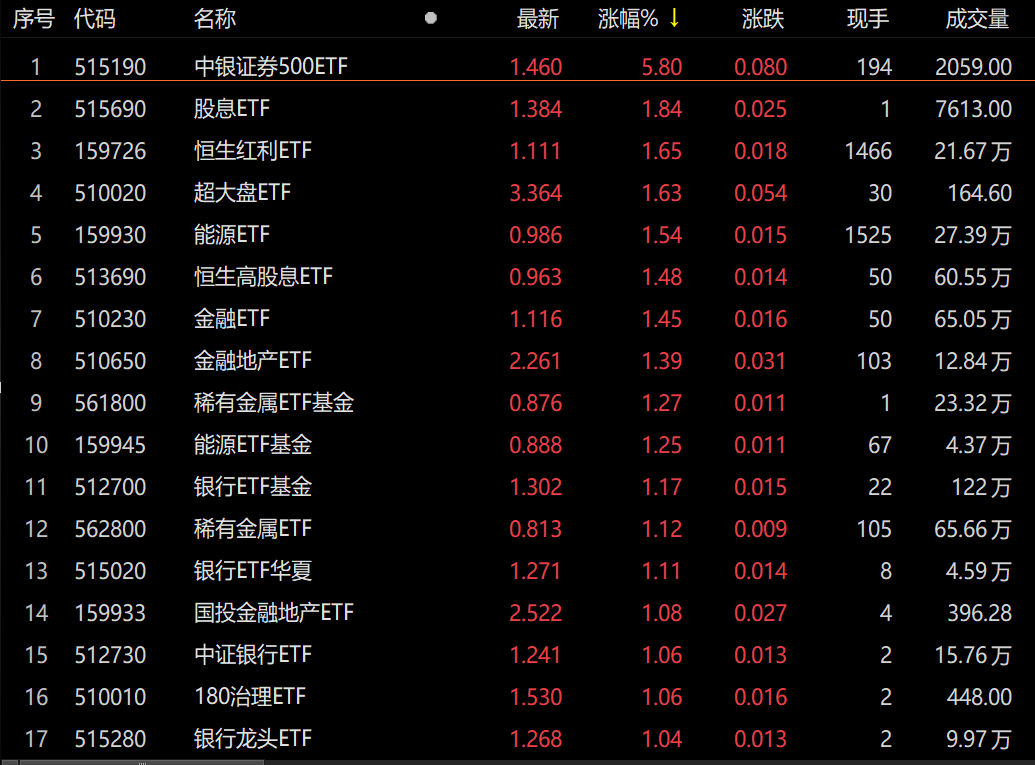 市场105只ETF出现上涨 中银证券今日涨幅高达5.80% 2月11日,资本邦了解到,本周最后一个交易日,A股三大指数震荡走低,截至今日收盘,沪指跌0 66%,深证成指跌1 55%,创业板指跌2 84%。盘面
市场105只ETF出现上涨 中银证券今日涨幅高达5.80% 2月11日,资本邦了解到,本周最后一个交易日,A股三大指数震荡走低,截至今日收盘,沪指跌0 66%,深证成指跌1 55%,创业板指跌2 84%。盘面 -
 立中集团拟投建大冶汽车轮毂基地 总投资额6亿元 80后董事长臧永兴掌舵8个月后,立中集团在湖北的投资有了大动作。2月8日晚间,立中集团(300428 SZ)公告称,拟在湖北黄石投建大冶汽车轮毂生
立中集团拟投建大冶汽车轮毂基地 总投资额6亿元 80后董事长臧永兴掌舵8个月后,立中集团在湖北的投资有了大动作。2月8日晚间,立中集团(300428 SZ)公告称,拟在湖北黄石投建大冶汽车轮毂生 -
 MSCI多类中国指数调整标的 A股涉及这些调整 2月10日,资本邦了解到,国际指数编制公司MSCI公布了其2022年2月的指数季度调整结果,本次调整结果将于2022年2月28日收盘后生效。在本次调
MSCI多类中国指数调整标的 A股涉及这些调整 2月10日,资本邦了解到,国际指数编制公司MSCI公布了其2022年2月的指数季度调整结果,本次调整结果将于2022年2月28日收盘后生效。在本次调
-
中国抗体-B(03681.HK):SM17新药研究申请获FDA受理 中国抗体-B(03681 HK)宣布,于2022年2月11日(美国东部当地时间),公司已就治疗哮喘的第一类(First-in-Class)治疗产品SM17(注射用人源化抗IL17R
-
京基智农接受5家机构调研!短期主力资金净流出 或存在资金分歧 京基智农于2022年2月15日接受5家机构调研。其中基金管理公司3家,证券公司2家,基于此调研事件,我们发现最近5个交易日,该公司的主力资金流向
-
威派格:约3.38亿股限售股2月22日解禁 占比79.37% 威派格(SH603956,收盘价:15 59元)2月16日晚间发布公告称,公司限售股份约3 38亿股将于2022年2月22日解禁并上市流通,占公司总股本比例为79 3
-
俞敏洪称新东方度过最安静寒假!然而 年前预亏超8亿美元 中新经纬2月16日电16日午间,新东方教育科技集团董事长兼首席执行官俞敏洪通过其个人微信公众号发布文章《老俞闲话丨一切都会更美好!》...
-
申通快递:2021年年底公司产能日均已突破4000万件整数关口 【申通快递:2021年年底公司产能日均已突破4000万件整数关口】申通快递(002468 SZ)2月16日表示,公司近些年持续强化基础设施建设,构建稳定运
-
芯朋微业绩快报:2021年净利同比增101.8% 【芯朋微业绩快报:2021年净利同比增101 8%】芯朋微(688508)2月16日晚间发布业绩快报,2021年实现营业收入7 53亿元,同比增长75 44%;净利润2
-
中国银河证券维持牧原股份推荐评级:股权激励彰显发展信心 龙头优势显著 中国银河02月16日发布研报称,维持牧原股份(002714 SZ,最新价:58 25元)推荐评级。评级理由主要包括:1)股权激励计划彰显未来发展信心;2)21
-
比依股份:2月18日在上交所上市 股票代码603215 比依股份2月16日晚间披露上市公告书,公司股票将于2022年2月18日在上海证券交易所上市。股票简称为比依股份。股票代码为603215。本次公开发行
-
力合微接受2家机构调研!短期主力资金净流入 市场资金或早已察觉 力合微于2022年2月11日接受2家机构调研。其中基金管理公司2家,基于此调研事件,我们发现最近5个交易日,该公司的主力资金流向呈现净买入131 4
-
骏东控股(08277.HK)拟4770.78万港元出售CD Enterprises全部股份 骏东控股(08277 HK)公告,于2022年2月16日,公司(即卖方)与买方FaithSinoVenturesLimited订立买卖协议,据此,买方有条件同意购买,而公司有条
-
富临精工:拟与宁德时代签署补充协议 将持有公司20%股权 【富临精工:拟与宁德时代签署补充协议将持有公司20%股权】富临精工公告,宁德时代与公司签署《补充协议》。宁德时代拟进一步对江西升华...
-
据越南青年报:越南将从3月15日起放松对国际旅游的限制 据越南青年报:越南将从3月15日起放松对国际旅游的限制
-
部分锂电材料报价继续上涨,电池级碳酸锂均价站上43万元/吨 部分锂电材料报价继续上涨,电池级碳酸锂均价站上43万元 吨;
-
陕西:2022年全省生态环境工作要点 陕西:2022年全省生态环境工作要点;
-
法国外贸银行:日本央行最终可能将收益率曲线控制目标调升至1% 法国外贸银行:日本央行最终可能将收益率曲线控制目标调升至1%;
-
SGS:马来西亚2月1日至15日棕榈油出口507673吨 SGS:马来西亚2月1日至15日棕榈油出口507673吨
-
俄“加马列亚”中心主任表示,该中心研制的鼻喷新冠疫苗不含活性病毒,因此不会给... 俄“加马列亚”中心主任表示,该中心研制的鼻喷新冠疫苗不含活性病毒,因此不会给机体带来危险。
-
共同社:七国集团准备2月中旬召开紧急外长会议 共同社:七国集团准备2月中旬召开紧急外长会议
-
白酒股震荡走强,金种子酒涨超9%,青海春天、巨力索具、盘江股份、岩石股份、金徽... 白酒股震荡走强,金种子酒涨超9%,青海春天、巨力索具、盘江股份、岩石股份、金徽酒跟涨
-
机构分析:趋势利好比特币、以太坊,而非原油 机构分析:趋势利好比特币、以太坊,而非原油;
-
1月份我国民航运输生产总体继续恢复 1月份我国民航运输生产总体继续恢复;
-
据卫星新闻援引消息人士称,俄罗斯不打算将其驻乌克兰大使馆从基辅迁出 据卫星新闻援引消息人士称,俄罗斯不打算将其驻乌克兰大使馆从基辅迁出
-
印尼央行行长warjiyo:印尼的直接外汇结算在2021年达到25.3亿美元 印尼央行行长warjiyo:印尼的直接外汇结算在2021年达到25 3亿美元
-
市场震荡新基金发行市场遭冷遇 2月已有2只新基金公告募集失败 中国网财经2月16日讯(记者张明江)日前同泰基金发布公告,旗下同泰同享混合型证券投资基金募集失败,这是2月份第二只公告募集失败的基金。昨日(
-
印尼央行行长warjiyo:我们相信印尼的经济正在复苏 印尼央行行长warjiyo:我们相信印尼的经济正在复苏
-
A股三大指数震荡整理 基建板块掀起涨停潮 【收盘播报】A股三大指数今日全天维持震荡整理态势,最终沪指收盘上涨0 57%,收报3465 83点;深证成指上涨0 23%,收报13376 36点;创业板指上
-
湘财证券:多头出现罕见大规模集中躁动! 【湘财证券:多头出现罕见大规模集中躁动!】今日两市股指跳空高开,之后沪指震荡走高至中午收盘,创业板早盘先行下探,9:45时见全日最低点后
-
印尼央行行长warjiyo:印尼将继续扩大本币结算项目 印尼央行行长warjiyo:印尼将继续扩大本币结算项目
-
容维证券刘思山:指数仍将震荡上扬 【容维证券刘思山:指数仍将震荡上扬】在美国股市上涨的背景下,今日沪深两市开盘呈现高开,生态园林、绿色建筑概念强劲拉升,设计咨询...
-
和信投顾:股指缩量震荡走高 【和信投顾:股指缩量震荡走高】周三A股在外围大涨影响之下股价高开之后震荡走高,全天人气逐渐恢复中,但力度有限,昨日强势的创业板今...
热门资讯
-
 顶流不牛了 景顺长城刘彦春正式掉出“千亿”梯队 今年市场走弱,令不少明星基金经理...
顶流不牛了 景顺长城刘彦春正式掉出“千亿”梯队 今年市场走弱,令不少明星基金经理... -
 蓝筹股上涨赛道股大跌 A股呈现明显分化走势 虎年首周,A股呈现明显的分化走势...
蓝筹股上涨赛道股大跌 A股呈现明显分化走势 虎年首周,A股呈现明显的分化走势... -
 信达生物股价大幅拉升至34.25港元 被要求补充额外临床试验 2月11日,资本邦了解到,港股公司...
信达生物股价大幅拉升至34.25港元 被要求补充额外临床试验 2月11日,资本邦了解到,港股公司... -
 市场105只ETF出现上涨 中银证券今日涨幅高达5.80% 2月11日,资本邦了解到,本周最后...
市场105只ETF出现上涨 中银证券今日涨幅高达5.80% 2月11日,资本邦了解到,本周最后...
文章排行
图赏
-
 原阳县“四大优势”吸引团餐企业落户 推动团餐行业高质量发展 还记得新乡7·20抗洪救灾期间,安...
原阳县“四大优势”吸引团餐企业落户 推动团餐行业高质量发展 还记得新乡7·20抗洪救灾期间,安... -
 拓荆科技针对科创板第二轮问询相关问题进行问询回复 盈利能力不足、产品类型单一且周转...
拓荆科技针对科创板第二轮问询相关问题进行问询回复 盈利能力不足、产品类型单一且周转... -
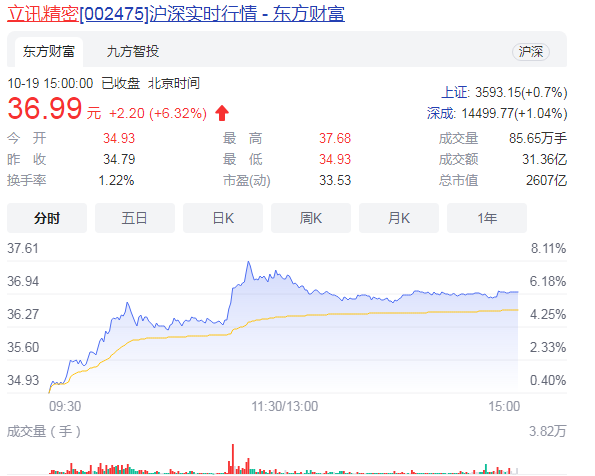 立讯精密涨6.32%目前报价36.99元 这家企业主要是干什么的? 据最新消息显示,立讯精密涨6 32%...
立讯精密涨6.32%目前报价36.99元 这家企业主要是干什么的? 据最新消息显示,立讯精密涨6 32%... -
 国漫多利好迈入黄金期 头部动漫公司扎堆IPO 今年以来,动漫市场绽放异彩。暑期...
国漫多利好迈入黄金期 头部动漫公司扎堆IPO 今年以来,动漫市场绽放异彩。暑期...