九安医疗:子公司iHealth新冠抗原快检产品获美EUA授权
九安医疗旗下产品再获美国EUA授权。
1月16日,天津九安医疗电子股份有限公司(九安医疗,002432)公告称,公司美国子公司 iHealth Labs Inc。的新型冠状病毒(SARS-CoV-2)抗原快速检测 POC(Point Of Care)专业版试剂盒(胶体金免疫层析法)获得应急使用授权(EUA),并收到了美国食品药品监督管理局(FDA)向iHealth美国发送的授权信。
九安医疗称,该产品获得美国应急使用授权(EUA)后,可在美国公共卫生健康应急状态期间,在美国和认可美国FDA EUA的国家/地区使用。
过去两个月来,九安医疗已经连续收获了27个涨停,股价从不到7元上涨到超75元,股价不断创造新高,累计涨幅超过1000%,成为名副其实的“妖股”。
九安医疗暴涨的源头正是新冠检测试剂盒。
九安医疗公告称,继2021年11月6日获得了iHealth新冠抗原家用自测OTC试剂盒的美国FDA EUA授权后,现获得了iHealth新冠抗原快速检测POC专业版试剂盒(iHealth COVID-19 Antigen Rapid Test Pro)的美国FDA EUA授权。该产品须按照产品使用说明,由专业医护人员或现场护理场景下能够熟练使用该试剂盒产品的人员采集前鼻腔拭子样本进行测试操作,15分钟可出结果,可供专业医护人员及现场护理(point of care)场景下能够熟练使用该试剂盒产品的人员在新冠肺炎的筛查工作中使用。
16日当天,九安医疗还发布股票交易异常波动暨风险提示公告。
九安医疗指出,公司美国子公司与美国纽约州,美国马萨诸塞州,以及美国HHS(由美国ACC代表执行)的合同及订单执行过程中受当地疫情变化、政策变化、公司供应链能力变化、物流运输风险以及不可预计或不可抗力等因素的影响,可能存在合同或订单无法如期或全部履行的风险。
公告称,需特别指出的是,美国政府有权随时因自身因素中止公司美国子公司与美国HHS(由美国ACC代表执行)签订的合同,该合同是否能够完全执行存在不确定性。
(文章来源:澎湃新闻)
-
 龙津药业股价莫名大增 大股东复制“割韭菜”模式 股价离奇大涨,大股东及实控人高位套现,樊献俄试图复制两年前的割韭菜模式。今年1月12日,二级市场上,龙津药业(002750 SZ)再度强势涨停。
龙津药业股价莫名大增 大股东复制“割韭菜”模式 股价离奇大涨,大股东及实控人高位套现,樊献俄试图复制两年前的割韭菜模式。今年1月12日,二级市场上,龙津药业(002750 SZ)再度强势涨停。 -
 中信证券发布业绩快报:2021年实现营业收入765.7亿 归母净利润229.79亿 1月12日,中信证券发布业绩快报,快报显示,2021年中信证券实现营业收入765 7亿元,同比增长40 8%;实现归属于母公司股东的净利润229 79亿元
中信证券发布业绩快报:2021年实现营业收入765.7亿 归母净利润229.79亿 1月12日,中信证券发布业绩快报,快报显示,2021年中信证券实现营业收入765 7亿元,同比增长40 8%;实现归属于母公司股东的净利润229 79亿元 -
 银河证券A股可转换债券发行规模缩小到78亿 比原拟定金额减少32亿 1月12日,中国银河证券股份有限公司(以下称银河证券)发布公告表示,公司董事会会议审议通过了关于调整银河证券公开发行A股可转换公司债券发
银河证券A股可转换债券发行规模缩小到78亿 比原拟定金额减少32亿 1月12日,中国银河证券股份有限公司(以下称银河证券)发布公告表示,公司董事会会议审议通过了关于调整银河证券公开发行A股可转换公司债券发 -
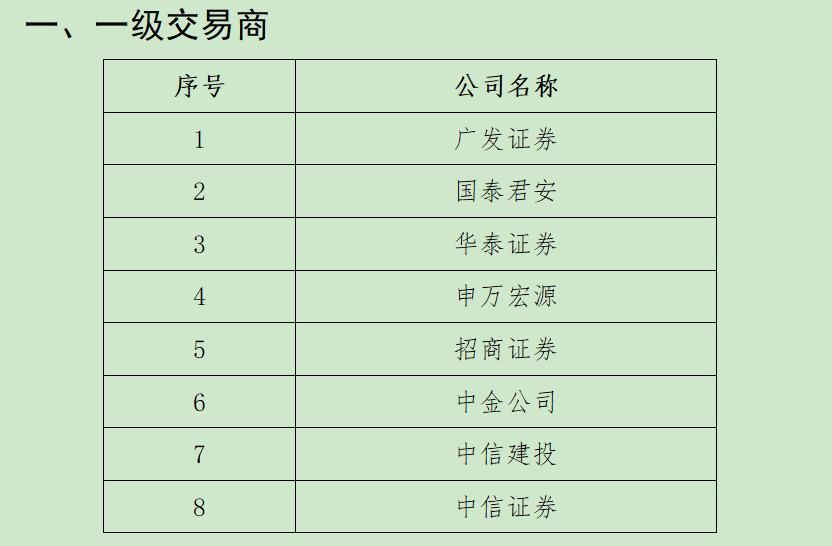 两期场外期权业务二级交易商新增名单接连公布 1月12日,资本邦了解到,开年前后,中国证券业协会接连公布两期场外期权业务二级交易商新增名单。其中,第十三期,新增北京高华证券和西南
两期场外期权业务二级交易商新增名单接连公布 1月12日,资本邦了解到,开年前后,中国证券业协会接连公布两期场外期权业务二级交易商新增名单。其中,第十三期,新增北京高华证券和西南 -
 圆通速递预盈超20亿增13.2% 单票收入大幅改善 持续推进数字化转型,圆通速递业绩增长超预期。1月10日,圆通速递(600233 SH)发布业绩预告,预计2021年1-12月归属上市公司股东的净利润20亿
圆通速递预盈超20亿增13.2% 单票收入大幅改善 持续推进数字化转型,圆通速递业绩增长超预期。1月10日,圆通速递(600233 SH)发布业绩预告,预计2021年1-12月归属上市公司股东的净利润20亿 -
 公募核心投研人士展发表2022年关注的投资机会 1月11日,资本邦了解到,日前,多家公募旗下核心投研人士发表2022年关注的投资机会,面对市场短期大幅波动,需要加强基本面研究,精选个股
公募核心投研人士展发表2022年关注的投资机会 1月11日,资本邦了解到,日前,多家公募旗下核心投研人士发表2022年关注的投资机会,面对市场短期大幅波动,需要加强基本面研究,精选个股
-
九安医疗:子公司iHealth新冠抗原快检产品获美EUA授权 九安医疗旗下产品再获美国EUA授权。1月16日,天津九安医疗电子股份有限公司(九安医疗,002432)公告称,公司美国子公司iHealthLabsInc。的新型
-
晶科能源17日启动申购!全球光伏龙头将登科创板 晶科能源即将登陆科创板。1月13日晚,晶科能源披露发行公告,发行价格为5元 股,拟公开发行20亿股,占公开发行后总股本的20%,申购日期为1月17
-
益客食品:1月18日在深交所上市 股票代码301116 益客食品1月16日晚间披露上市公告书,公司股票将于2022年1月18日在深圳证券交易所创业板上市。股票简称为益客食品。股票代码为301116。2021年
-
巴拿马籍船舶在汕头享受69万元退税款 “我们昨天向海关提交了申请,今天就收到船舶吨税退税,所有手续全部网上‘搞定’,真的太方便了。”近日,汕头中远海运船务代理有限公...
-
厨具变姜糖?147吨不实出口货物被汕头海关查获 出口申报为“不锈钢厨具”,实则运输凉果、糖果等食品和发蜡。近日,汕头海关所属汕头港海关对一报关企业代理申报出口的货物实施查验,...
-
诺德股份拟投建10万吨铜箔材料新生产基地项目 诺德股份公告,公司与湖北省黄石市黄石经济技术开发区管理委员会& 183;铁山区政府拟签署《项目投资合同书》,投资建设诺德10万吨铜箔材...
-
苏州银行2021年归母净利润31.01亿元 同比增长20.57% 1月16日,苏州银行发布2021年度业绩快报。2021年,该行实现营收108 31亿元,较上年同期增长4 51%;实现归属于上市公司股东的净利润31 01亿元,
-
光威复材业绩快报:2021年净利同比增长18.31% 财联社1月16日电,光威复材披露2021年度业绩快报,报告期内,公司实现营业总收入26 07亿元,同比增长23 25%,归母净利润7 59亿元,同比增长18
-
国金证券首予张小泉增持评级:“老字号”焕发新生 成长有望提速 目标价26.1元 国金证券01月16日发布研报称,首予张小泉(301055 SZ,最新价:23 3元)增持评级,目标价格为26 1元。评级理由主要包括:1)中华老字号刀剪企业—
-
裕兴股份:2021年净利同比预增45%至65% 【裕兴股份:2021年净利同比预增45%至65%】裕兴股份披露业绩预告,预计2021年度归母净利润2 26亿元至2 58亿元,同比增长45%至65%。报告期内,
-
贝达药业:BPI-371153胶囊获得临床试验批准通知书 【贝达药业:BPI-371153胶囊获得临床试验批准通知书】贝达药业1月16日晚间公告,近日,公司收到国家药品监督管理局(NMPA)签发的《药物临床试验
-
丝路视觉:2021年净利同比预增2.98%至27.83% 丝路视觉1月16日晚间公告,预计2021年归属于上市公司股东的净利润6240 98万元至7747 43万元,同比增长2 98%至27 83%。2021年非经常性损益预计
-
华西策略:分水岭或在春节之后 蓄势待发 一、海外市场:美国通胀继续走高,美债收益率升至两年高位。2021年12月美国CPI同比上涨7 0%(前值6 8%),连续第19个月上涨,续创1982年以来新高
-
预增!博腾股份:预计2021年度净利润为5亿元~5.32亿元 同比增长54%~64% 博腾股份(SZ300363,收盘价:79 7元)1月16日晚间发布业绩预告,预计2021年归属于上市公司股东的净利润5亿元~5 32亿元,同比增长54%~64%。业绩
-
豪悦护理股东拟减持不超3%公司股份 豪悦护理公告,持股4 26714%的股东温州瓯泰计划通过集中竞价交易方式减持公司股份不超过4,795,149股,即不超过公司总股本的3%。
-
迈为股份:预计2021年净利同比增长47.05%-72.4% 【迈为股份:预计2021年净利同比增长47 05%-72 4%】迈为股份公告,预计2021年归母净利为5 8亿元–6 8亿元,同比增长47 05%-72 4%。报告期内,
-
迈为股份:预计2021年净利同比增长47.05%-72.4% 1月16日,迈为股份公告,预计2021年归母净利为5 8亿元–6 8亿元,同比增长47 05%-72 4%。报告期内,公司主营产品太阳能电池丝网印刷设备销量稳
-
中泰化学:筹划重大资产重组 股票停牌 中泰化学公告,公司拟发行股份及可转换公司债券的方式购买新疆中泰(集团)有限责任公司等股东持有的新疆美克化工股份有限公司部分或全部...
-
伦敦金融城市长Alderman Vincent Keaveny:绿色转型需要政府和私营部门之间协调一致 1月15日,伦敦金融城市长AldermanVincentKeaveny在全球财富管理论坛上海苏河湾峰会致辞时表示,绿色转型需要政府和私营部门之间协调一致。Alde
-
国盛策略:本轮“高切低”结束了吗? 2022开年以来,除“开门不红”之外,市场的一个重要特征就是高低估值的切换。从节奏与逻辑来看,本轮高低估值切换与2021Q3存在一定的可...
-
数据图解丨2020年全国农业及相关产业增加值达166900亿元 占GDP16.47%! 农业统计是反映农业农村经济活动的“晴雨表”。1月14日,针对近期公开的2020年全国农业及相关产业增加值数据,国家统计局发布了国家统计...
-
九芝堂:连锁药店数量每年保持约10%的增长速度 最近这两个月,作为传统中药龙头的九芝堂股价从8 40涨到了10 38元(截至1月14收盘),增幅达23 5%,吸金效应明显。九芝堂2021三季报显示,公司主
-
曹宇:去年底基本完成资管业务过渡期整改任务 保本理财实现清零 在今日举行的全球财富管理论坛& 183;上海苏河湾峰会上,中国银保监会党委委员、副主席曹宇表示,银行业保险业已于2021年底基本完成资管...
-
西安市区出租车免除本月承包费和服务费 西安发布消息1月15日,西安市出租汽车管理处、西安出租汽车协会联合发布通知:西安市区所有出租汽车经营企业免除企业自有车辆(公户车)承包人20
-
电影《穿过寒冬拥抱你》上映第17天 票房突破8亿元 【电影《穿过寒冬拥抱你》上映第17天票房突破8亿元】1月16日,电影《穿过寒冬拥抱你》上映第17天,票房突破8亿元。截至发稿前,该片超越了本周
-
年货促销节“真香”来袭 来越秀一起虎虎生威欢购幸福年 距离虎年大年初一还有不到20天,越秀年货市场早已热闹起来。传统商超消费持续火热,一德路年货一条街红红火火。广百、华润万家等商超年...
-
不耽误港澳渔民返乡过节!湾仔边检升级执勤方案 据珠海市流渔办通报,2022年春节前将有近2000名港澳流动渔(船)民在市各渔港集中入境上岸,其中,洪湾中心渔港以自身国家级中心渔港建造标准的
-
广州一物流公司“套路”司机贷款买车 崭新货车却成负担 1月14日,林荣告诉记者,去年9月,自己在智联招聘上看到广州骏宇物流有限公司招聘货车司机,便去应聘司机岗位。面试时,该公司工作人员表示底
-
2022年江西“两会”时间来了 首设“代表通道”、“厅长通道” 1月15日下午,《每日经济新闻》记者从2022年江西省“两会”新闻发布会上获悉,江西省政协十二届五次会议将于明日(16日)下午开幕,这也意...
-
兴证策略:“mini版2014”正在酝酿 时机取决于宽信用进程 回顾:2021年10月中旬我们判断主线将回归成长,科技科创将吹响反攻号角。2021年11月10日在市场大幅震荡中,我们判断跨年行情即将展开。展望:
热门资讯
-
 龙津药业股价莫名大增 大股东复制“割韭菜”模式 股价离奇大涨,大股东及实控人高位...
龙津药业股价莫名大增 大股东复制“割韭菜”模式 股价离奇大涨,大股东及实控人高位... -
 中信证券发布业绩快报:2021年实现营业收入765.7亿 归母净利润229.79亿 1月12日,中信证券发布业绩快报,...
中信证券发布业绩快报:2021年实现营业收入765.7亿 归母净利润229.79亿 1月12日,中信证券发布业绩快报,... -
 银河证券A股可转换债券发行规模缩小到78亿 比原拟定金额减少32亿 1月12日,中国银河证券股份有限公...
银河证券A股可转换债券发行规模缩小到78亿 比原拟定金额减少32亿 1月12日,中国银河证券股份有限公... -
 两期场外期权业务二级交易商新增名单接连公布 1月12日,资本邦了解到,开年前后...
两期场外期权业务二级交易商新增名单接连公布 1月12日,资本邦了解到,开年前后...
文章排行
图赏
-
 原阳县“四大优势”吸引团餐企业落户 推动团餐行业高质量发展 还记得新乡7·20抗洪救灾期间,安...
原阳县“四大优势”吸引团餐企业落户 推动团餐行业高质量发展 还记得新乡7·20抗洪救灾期间,安... -
 拓荆科技针对科创板第二轮问询相关问题进行问询回复 盈利能力不足、产品类型单一且周转...
拓荆科技针对科创板第二轮问询相关问题进行问询回复 盈利能力不足、产品类型单一且周转... -
 立讯精密涨6.32%目前报价36.99元 这家企业主要是干什么的? 据最新消息显示,立讯精密涨6 32%...
立讯精密涨6.32%目前报价36.99元 这家企业主要是干什么的? 据最新消息显示,立讯精密涨6 32%... -
 国漫多利好迈入黄金期 头部动漫公司扎堆IPO 今年以来,动漫市场绽放异彩。暑期...
国漫多利好迈入黄金期 头部动漫公司扎堆IPO 今年以来,动漫市场绽放异彩。暑期...