康弘药业前三季度净利增12.8% 核心产品出海“遇挫” 股价年内跌超60%
核心产品康柏西普“出海”失败的康弘药业(002773.SZ)三季报表现如何?
财务数据显示,康弘药业2021年前三季度营收28.45亿元,同比增幅21.16%,净利润6.53亿元,同比增幅12.8%,扣非净利润5.86亿元,同比也有12.26%的增幅。要知道2020年全年康弘药业还亏损了2.7亿元。
据悉,康弘药业主营业务为药品(包括生物制品、中成药、化学药)和医疗器械(主要是眼科医疗器械)的研发、生产与销售,目前上市产品主要为:康柏西普眼用注射液、松龄血脉康胶囊、舒肝解郁胶囊、渴络欣胶囊、胆舒胶囊、一清胶囊、盐酸文拉法辛缓释片、阿立哌唑口崩片、阿立哌唑口服溶液、枸橼酸莫沙必利片、枸橼酸莫沙必利分散片、右佐匹克隆片等十八个药品和两个医疗器械。
说起康柏西普眼用注射液事件,恐怕是康弘药业2021年所经历的最大的事。
4月10日,康弘药业披露,公司曾在2018年5月启动关于“一项多中心、双盲、随机、剂量范围试验,评估康柏西普眼用注射液治疗新生血管性年龄相关性黄斑变性患者的疗效和安全性”临床试验项目(下称PANDA试验)。2020年9月25日,PANDA试验完成全部受试者的第36周主要终点访视。
然而2020年初以来,全球突发公共卫生事件、外部环境变化等不利因素对临床研究造成了极大的困难和影响。虽然公司为此追加了大量人力、财力,保留和保护受试患者以减少不利影响,努力使PANDA试验能按时推进。但公司无法在揭盲前获悉各组受试者的获益情况,实际影响更难以评估。现在已经揭盲的阶段性分析表明,全球公共卫生事件对本研究的影响大大超过公司的预期,包括各国不断出台的各种管控措施等因素使得大量受试者脱落、失访、超窗,完全符合PANDA试验给药方案的病例已逐步降低到不足入组病例的40%。特别是国际航运和出行限制的阻碍,使得需要全程冷链配送的试验药品的质量控制以及需要去医院现场临床监查和稽查,都变得格外艰难。此外,高达68个试验中心,有一半以上的受试者视力在注射后较基线变化等于甚至低于零,这与试验药物既往的临床研究以及真实世界大量的使用经验有很大差异。
最终于2021年4月9日,PANDA试验科学指导委员会召开专题会议,基于上述环境下产生的数据进行了中期评议。委员会认为本试验在全球公共卫生事件期间,大量受试者偏离试验规定的给药方案;康柏西普在试验中表现出了良好的安全性;在亚裔人群的亚组分析中,1mg康柏西普每三个月注射一次的剂量组疗效表现可能优于整体。同时,对于试验药物和冷链供应可能受到的影响深表关切,建议开展后续的调查研究。但委员会认为PANDA试验未能达到预期目标,建议公司停止PANDA试验。公司经过慎重研究,也最终决定停止。
消息一出,市场炸锅,股价直接3个“一字跌停”先跌为敬。再加上此前3月29日康弘药业曾有披露过一些进展信息,当时就已引起了一波累计20%的下跌,如此叠加之下,康弘药业股价腰斩。并且截至目前,股价也仍然在底部趴着。今年以来,该股股价累计下跌61.52%。
但需要指出的是,后续的6月份,其实康弘药业曾收到了国家药品监督管理局签发的《药物临床试验批准通知书》,同意开展临床试验。但此消息却并未引起二级市场相应的反响。如今三季报披露,也能窥见其缘由。
来源:公告
据介绍, 康柏西普眼用注射液是公司全资子公司康弘生物自主研发的具有完全自主知识产权的1类生物创新药,该产品能有效地与血管及组织中的VEGF结合,阻断由VEGF介导的促进新生血管出芽和生长的信号传递。康柏西普眼用注射液于2013年获批用于治疗湿性年龄相关性黄斑变性(nAMD),2017年获批用于治疗继发于病理性近视脉络膜新生血管引起的视力损伤(pmCNV),2019年获批用于治疗继发于糖尿病黄斑水肿(DME)引起的视力损害。
从数据来看,截至2021年3月31日时,康弘药业的股东户数为3.27万户,但经历了诸多之后,截至6月底,股东户数就已经变为7.37万户。筹码出现了明显松动,持股较大的一些股东选择了离场。虽又经过了一个季度,但截至2021年9月底,康弘药业的股东户数仍然有6.28万户,户数虽有所减少,但远不及大跌之前。
(文章来源:界面新闻)
-
 前三季度完成交通固定资产投资25632亿元 同比增长2% 记者今天从交通运输部获悉,前三季度,交通运输经济运行总体平稳,交通投资、货运量、港口货物吞吐量两年平均增速均在6%左右,其中三季度受
前三季度完成交通固定资产投资25632亿元 同比增长2% 记者今天从交通运输部获悉,前三季度,交通运输经济运行总体平稳,交通投资、货运量、港口货物吞吐量两年平均增速均在6%左右,其中三季度受 -
 1-9月份第一产业投资10395亿元 同比增长14.0% 据国家统计局官网消息,1-9月份,全国固定资产投资(不含农户)397827亿元,同比增长7 3%;比2019年1-9月份增长7 7%,两年平均增长3 8%。其中
1-9月份第一产业投资10395亿元 同比增长14.0% 据国家统计局官网消息,1-9月份,全国固定资产投资(不含农户)397827亿元,同比增长7 3%;比2019年1-9月份增长7 7%,两年平均增长3 8%。其中 -
 1-8月河南省货物贸易保持高速增长 商务运行稳中有进 据河南省商务厅官网消息,2021年1-8月,全省货物贸易保持高速增长,招商引资保持增长态势,消费品市场恢复态势放缓,对外投资大幅增长,商
1-8月河南省货物贸易保持高速增长 商务运行稳中有进 据河南省商务厅官网消息,2021年1-8月,全省货物贸易保持高速增长,招商引资保持增长态势,消费品市场恢复态势放缓,对外投资大幅增长,商 -
 医药板块投资性价比显现 基金公司密集调研医药上市公司 12月14日,资本邦了解到,随着年内的持续调整,此前一直处于高估值的医药板块投资性价比显现,因此基金公司对相关主题基金的布局速度加快。
医药板块投资性价比显现 基金公司密集调研医药上市公司 12月14日,资本邦了解到,随着年内的持续调整,此前一直处于高估值的医药板块投资性价比显现,因此基金公司对相关主题基金的布局速度加快。 -
 稳增长预期确认 中信证券:跨年蓝筹行情预计将延续数月 12月13日,资本邦了解到,上周(12月6日—12月10日),A股在央行宣布全面降准0 5个百分点后,迎来震荡上行,上证指数周涨幅1 63%,深证成指全
稳增长预期确认 中信证券:跨年蓝筹行情预计将延续数月 12月13日,资本邦了解到,上周(12月6日—12月10日),A股在央行宣布全面降准0 5个百分点后,迎来震荡上行,上证指数周涨幅1 63%,深证成指全 -
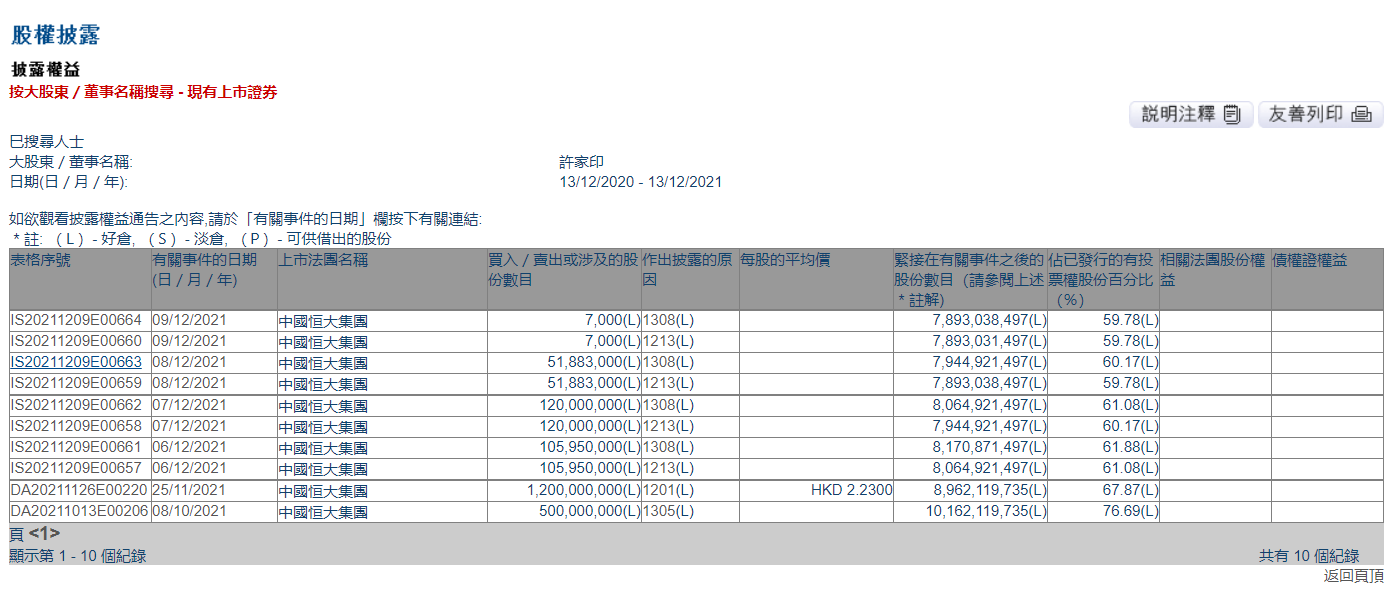 许家印在中国恒大持股比例从61.88%下降至59.78% 12月13日,资本邦了解到,港交所文件显示,依据强制处置事项,12月6日、12月7日、12月8日、12月9日,许家印持续被强制卖出中国恒大1 06亿股
许家印在中国恒大持股比例从61.88%下降至59.78% 12月13日,资本邦了解到,港交所文件显示,依据强制处置事项,12月6日、12月7日、12月8日、12月9日,许家印持续被强制卖出中国恒大1 06亿股
-
国联股份:全国营销体系建设项目是建立健全一个基本满足多多电商平台属地服务的全... 每经AI快讯,有投资者在投资者互动平台提问:潘总您好,IPO募集的资金中有7940万元用于全国营销体系建设项目,麻烦潘总介绍下这个项目。目前进
-
奇安信吴云坤:零信任是数据安全的必然选择和创新方向 “数据安全是数字化时代关基保护的核心和关键。”12月16日,在由中国计算机学会计算机安全专委会数据安全工作组举办的“零信任分论坛”...
-
中矿资源:年内可完成3000吨/年扩建至6000吨/年的氟化锂技改项目 【中矿资源:年内可完成3000吨 年扩建至6000吨 年的氟化锂技改项目】中矿资源(002738)12月17日在互动平台表示,根据目前公司工作进展情况来看
-
恒生科指又创新低!港股究竟有多“便宜”?券商:明年配置这些板块! 恒生科指又创新低!港股究竟有多“便宜”?券商:明年配置这些板块!新经济是港股胜负手。
-
广东省政府副秘书长、省政数局局长杨鹏飞到茂名调研“办事不出村”改革工作 日前,广东省政府副秘书长、省政数局局长杨鹏飞带队到茂名调研,深入茂名高州云潭镇读岗村了解“办事不出村”改革工作情况。杨鹏飞一行...
-
大鹏街道蝶变记②丨一轴两湾多点集中发力 大鹏街道推动经济高质量发展 在加快“生态立区经济强区”建设,全面开启大鹏高质量发展的征途上,大鹏办事处全面贯彻新发展理念,硬环境建设,软实力提升,锚定目标...
-
“网红神盘”不香了?深圳豪宅新盘大降温 此前曾遭疯抢 严控下购房者变理性 【“网红神盘”不香了?深圳豪宅新盘大降温此前曾遭疯抢严控下购房者变理性】隆冬时节,深圳的新房市场也寒意阵阵。备受市场瞩目的深圳...
-
菲达环保三度谋划资产重组背后:内幕交易、信披数据“打架”、疑借收购提升业绩 时隔近五个月,菲达环保(600526 SH)重大资产重组方案再出变数。12月16日晚间,菲达环保公告,拟向杭钢集团发行股份购买其所持有的紫光环保62 9
-
闷声发大财!今年这些海外上游厂商股价远远跑赢特斯拉 近两年,电动车行业无疑是全球投资市场最引人注目的行业之一,尤其是电动车领军企业特斯拉的股价猛涨尤其令人惊叹。不过今年,由于上游...
-
和信投顾:沪指早盘小幅低开 芯片股持续低迷 【和信投顾:沪指早盘小幅低开芯片股持续低迷】截止午间收盘,沪指跌0 9%,深成指跌1 35%,创业板指跌1 38%。北向资金方面,沪股通早盘净流出3
-
爱好成就大奖 山东购彩者淡定领走足彩107万元 11月12日,烟台龙口传出喜报,在足彩胜平负14场第21136期中,龙口购彩者中得一等奖一注、二等奖九注,奖金合计1077044元。中奖后,大奖得主迟
-
 花呗影响个人负债率吗 影响借款人个人负债率的因素还有哪些? 如今互联网发展越来越快速,市面上的小额贷款也越来越多。支付宝平台有不少小贷产品,大家所熟知的蚂蚁花呗。日前,有一个朋友询问,花呗影
花呗影响个人负债率吗 影响借款人个人负债率的因素还有哪些? 如今互联网发展越来越快速,市面上的小额贷款也越来越多。支付宝平台有不少小贷产品,大家所熟知的蚂蚁花呗。日前,有一个朋友询问,花呗影 -
白酒股午后持续走低 来伊份触及跌停 每经AI快讯,白酒股午后持续走低,来伊份触及跌停,贵州茅台、老白干酒、泸州老窖、皇台酒业、五粮液等跌超3%。
-
稀土永磁板块持续走低 【稀土永磁板块持续走低】正海磁材、英洛华、银河磁体、大地熊、有研新材、宁波韵升跌超5%。
-
宝泰隆:目前未有石墨负极业务 【宝泰隆:目前未有石墨负极业务】宝泰隆(601011)在互动平台表示,目前公司拥有的石墨矿正在办理采矿权证,尚未进行开采。公司目前未有石墨负
-
硅宝科技:光伏太阳能用胶已全面进入太阳能光伏组件、BIPV等多个领域 【硅宝科技:光伏太阳能用胶已全面进入太阳能光伏组件、BIPV等多个领域】硅宝科技(300019)在接受机构调研时表示,公司光伏太阳能用胶已全面进
-
万集科技发布混合固态128线车规级激光雷达 【万集科技发布混合固态128线车规级激光雷达】记者获悉,12月16日,在广州召开的世界智能汽车大会上,万集科技发布了混合固态128线车规级激光
-
借鉴历史,哪些刺激消费政策值得期待? 据新华社报道,2021年12月6日中共中央政治局召开会议,分析研究当前经济形势和经济工作,指出“实施好扩大内需战略,促进消费持续恢复”...
-
 彝人老家:深度根植贫困县,辐射带动你我他 凉山州位于四川西南边陲,广袤无垠,层峦叠嶂,北起大渡河,南临金沙江山山水水在亘古岁月中见证着沧海桑田。山高谷深、林峰苍茫,是典型的深度
彝人老家:深度根植贫困县,辐射带动你我他 凉山州位于四川西南边陲,广袤无垠,层峦叠嶂,北起大渡河,南临金沙江山山水水在亘古岁月中见证着沧海桑田。山高谷深、林峰苍茫,是典型的深度 -
才高兴了一天!美股科技巨头全线下挫 终究仍躲不开美联储紧缩风暴? 【才高兴了一天!美股科技巨头全线下挫终究仍躲不开美联储紧缩风暴?】中国有句老话:“是福不是祸,是祸躲不过”,对于那些本周手中握...
-
IDC头部玩家光环新网定增落定,兴证财通诺德再上获配名单,海通广发银河同参与,ID... 12月16日,IDC头部玩家光环新网发布了规模30亿元的定增结果公告。光环新网是业界领先的互联网综合服务提供商,主营业务为互联网数据中心服务(I
-
巨丰投顾:整理不改向好趋势 A股跨年行情仍值得期待 【巨丰投顾:整理不改向好趋势A股跨年行情仍值得期待】观点:宏观面看,尽管短期经济回升,但整体经济增速放缓,下行压力依然较大。不过...
-
巨丰投顾:科技股回调致A股走弱 跨年行情迎低吸机会 【巨丰投顾:科技股回调致A股走弱跨年行情迎低吸机会】周五,A股低开低走,创业板领跌。盘面上,电源设备、电网设备、采掘、电力、房地...
-
源达:震荡仍是当下市场主基调 【源达:震荡仍是当下市场主基调】今日沪深两市指数整体呈现震荡调整格局。三大指数早盘均低开低走,弱势格局明显。
-
元旦当日车票 18日就能购买 天津北方网讯:从铁路部门获悉,进入12月中旬,根据最新铁路火车票预售期规定,2022年元旦火车票提前15天开售。明天可购买2022年元旦当天的火
-
水泥价格高价区触顶徘徊 煤价大降提升四季度毛利 临近年底,本应是各地工程赶进度,水泥价格最高的时候,而今年旺季不旺,水泥价格已连续下跌超一个月,较10月价格最高时有明显回落。而...
-
央行副行长陈雨露:继续完善准入前国民待遇和负面清单管理制度 【央行副行长陈雨露:继续完善准入前国民待遇和负面清单管理制度】中国人民银行副行长陈雨露在《中国金融》杂志最新撰文称,继续完善准...
-
山科智能项目入选2021年全国智慧企业建设创新案例 【山科智能项目入选2021年全国智慧企业建设创新案例】山科智能(300897)17日消息,公司与大连德泰水务有限公司合作开发的《基于智慧水务综合平
-
“新希望系”计划控股红星乳业 持股比例或在51%—60% 【“新希望系”计划控股红星乳业持股比例或在51%—60%】近日,新希望乳业董事长席刚出任红星乳业董事职位,另有“新希望系”高管邱屿、...
-
巨丰投顾:整理不改向好趋势 A股跨年行情仍值得期待 【巨丰投顾:整理不改向好趋势A股跨年行情仍值得期待】观点:宏观面看,尽管短期经济回升,但整体经济增速放缓,下行压力依然较大。不过...
热门资讯
-
 前三季度完成交通固定资产投资25632亿元 同比增长2% 记者今天从交通运输部获悉,前三季...
前三季度完成交通固定资产投资25632亿元 同比增长2% 记者今天从交通运输部获悉,前三季... -
 1-9月份第一产业投资10395亿元 同比增长14.0% 据国家统计局官网消息,1-9月份,...
1-9月份第一产业投资10395亿元 同比增长14.0% 据国家统计局官网消息,1-9月份,... -
 1-8月河南省货物贸易保持高速增长 商务运行稳中有进 据河南省商务厅官网消息,2021年1-...
1-8月河南省货物贸易保持高速增长 商务运行稳中有进 据河南省商务厅官网消息,2021年1-... -
 医药板块投资性价比显现 基金公司密集调研医药上市公司 12月14日,资本邦了解到,随着年内...
医药板块投资性价比显现 基金公司密集调研医药上市公司 12月14日,资本邦了解到,随着年内...
文章排行
图赏
-
 拓荆科技针对科创板第二轮问询相关问题进行问询回复 盈利能力不足、产品类型单一且周转...
拓荆科技针对科创板第二轮问询相关问题进行问询回复 盈利能力不足、产品类型单一且周转... -
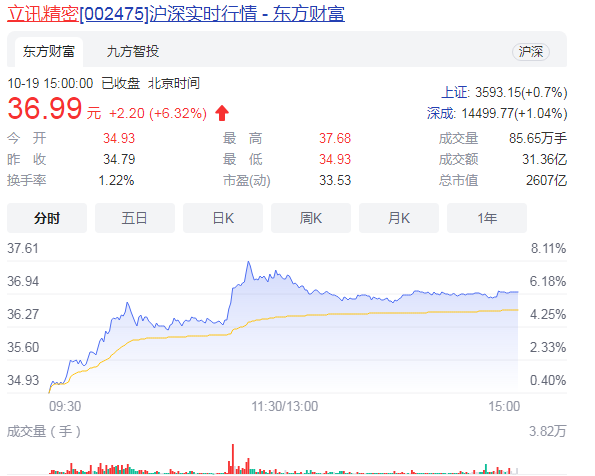 立讯精密涨6.32%目前报价36.99元 这家企业主要是干什么的? 据最新消息显示,立讯精密涨6 32%...
立讯精密涨6.32%目前报价36.99元 这家企业主要是干什么的? 据最新消息显示,立讯精密涨6 32%... -
 国漫多利好迈入黄金期 头部动漫公司扎堆IPO 今年以来,动漫市场绽放异彩。暑期...
国漫多利好迈入黄金期 头部动漫公司扎堆IPO 今年以来,动漫市场绽放异彩。暑期... -
 4月1日起 北京市燃油车不得占用充电专用泊位 充电站必须配专人巡检 今日,记者从北京市市场监管局网站...
4月1日起 北京市燃油车不得占用充电专用泊位 充电站必须配专人巡检 今日,记者从北京市市场监管局网站...